Von Jason Wasserman MD PhD FRCPC und Matt Cecchini MD PhD FRCPC
November 27, 2025
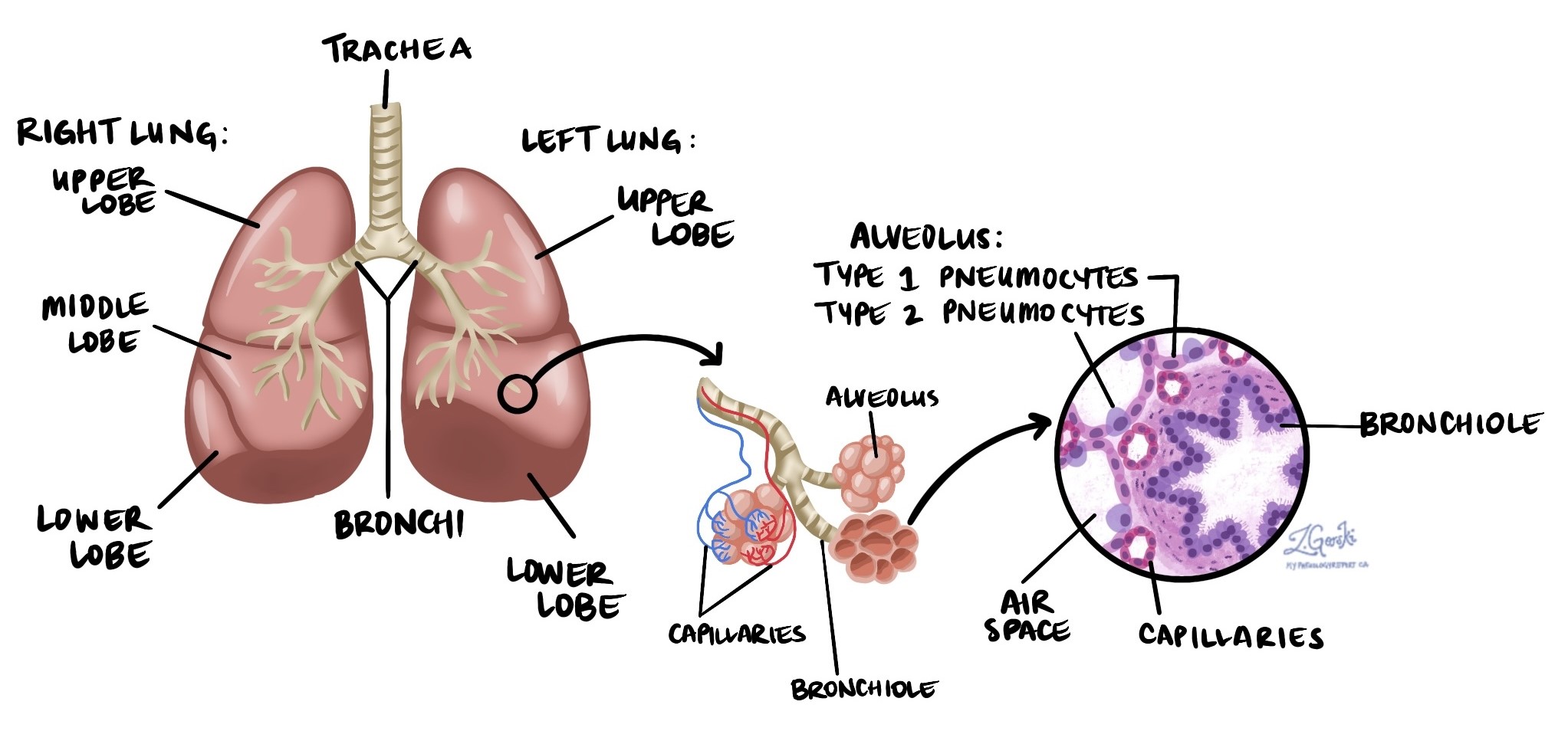
Adenokarzinom ist die häufigste Form von Lungenkrebs und macht etwa 40 % aller Lungenkrebsfälle in Nordamerika aus. Sie gehört zur Gruppe der Krebsarten, die als Lungenkrebs bekannt sind. nicht-kleinzelliger Lungenkrebs (NSCLC)Adenokarzinome entstehen in den Pneumozyten, den spezialisierten Zellen, die die winzigen Lungenbläschen, die Alveolen, auskleiden. In den Alveolen gelangt Sauerstoff ins Blut, und Kohlendioxid wird abgegeben.
Da Adenokarzinome häufig in der Nähe der äußeren Ränder der Lunge entstehen, können sie frühzeitig erkannt werden, wenn bildgebende Verfahren – wie Röntgenaufnahmen oder CT-Scans – einen kleinen Knoten oder eine Geschwulst zeigen.
Was verursacht ein Adenokarzinom in der Lunge?
Die häufigste Ursache für Lungenadenokarzinome ist Tabakkonsum. Dazu gehören Zigaretten, Zigarren und Pfeifen. Adenokarzinome können jedoch auch bei Menschen auftreten, die nie geraucht haben.
Weitere Ursachen und Risikofaktoren sind:
-
Radonbelastung.
-
Berufliche Belastungen, wie z. B. durch Asbest, Siliziumdioxid oder Dieselabgase.
-
Luftverschmutzung im Freien.
Diese Faktoren können Lungenzellen schädigen und mit der Zeit das Krebsrisiko erhöhen.
Was sind die Symptome eines Adenokarzinoms in der Lunge?
Die Symptome eines Lungenadenokarzinoms sind vielfältig. Manche Menschen haben keine Symptome, insbesondere im Frühstadium. Treten Symptome auf, können diese Folgendes umfassen:
-
Ein anhaltender oder sich verschlimmernder Husten.
-
Blut abhusten.
-
Brustschmerz.
-
Kurzatmigkeit.
-
Müdigkeit oder ungewollter Gewichtsverlust.
Wenn sich der Krebs auf andere Körperteile ausbreitet, hängen die Symptome vom betroffenen Bereich ab. Beispielsweise kann eine Ausbreitung auf die Knochen Schmerzen oder sogar eine pathologische Fraktur verursachen, also einen Knochenbruch, der durch die Schwächung des Knochengewebes durch den Krebs entsteht.
Welche Erkrankungen sind mit einem Adenokarzinom der Lunge verbunden?
Ein Adenokarzinom der Lunge kann aus präkanzerösen Zuständen wie beispielsweise folgenden entstehen:
-
Bei der atypischen adenomatösen Hyperplasie (AAH) handelt es sich um eine Erkrankung, bei der die Auskleidungszellen der Alveolen abnormal aussehen, aber nicht krebsartig sind.
-
Adenokarzinom in situ (AIS) ist eine nicht-invasive Krebsart, die auf die Innenfläche der Alveolen beschränkt ist und kleiner als 3 cm ist.
AIS kann sich zu einem invasiven Adenokarzinom entwickeln, wenn der Tumor größer als 3 cm wird oder wenn Krebszellen in das Stützgewebe unterhalb der Alveolarauskleidung eindringen.
Wie wird diese Diagnose gestellt?
Die Diagnose eines Adenokarzinoms beginnt, wenn bildgebende Verfahren einen verdächtigen Bereich in der Lunge zeigen. Zur Bestätigung der Diagnose wird eine... Biopsie Eine Biopsie dient der Entnahme einer kleinen Gewebeprobe. Sie kann mittels Nadelbiopsie, Bronchoskopie, endobronchialem Ultraschall (EBUS) oder Feinnadelaspiration (FNA) erfolgen. Die Gewebeprobe wird anschließend von einem Pathologen, einem Facharzt für die Diagnose von Krankheiten anhand von Gewebeproben, mikroskopisch untersucht.
Wird Krebs diagnostiziert, kann eine Operation zur Tumorentfernung empfohlen werden. Die Art des Eingriffs hängt von Größe und Lage des Tumors ab. Kleinere Tumoren in der Nähe der Körperoberfläche können mittels Keilresektion entfernt werden, während größere oder zentraler gelegene Tumoren eine Lobektomie oder sogar eine Pneumonektomie erforderlich machen können.
Nach der Entfernung untersucht der Pathologe den gesamten Tumor. Wichtige Merkmale sind:
-
Das Wachstumsmuster (histologischer Typ).
-
Ob sich der Krebs in das umliegende Lungengewebe ausgebreitet hat.
-
Ob sich die Ausbreitung über Lufträume erstreckt (STAS) ist vorhanden.
-
Ob Tumorzellen in Blutgefäße oder Lymphbahnen eingedrungen sind.
-
Ob der Tumor in das Brustfell eingewachsen ist.
-
Ob die Operationsränder tumorfrei sind.
-
Ob Lymphknoten Krebszellen enthalten.
Immunhistochemie (IHC)
Immunhistochemie Es handelt sich um einen speziellen Test, bei dem Antikörper, die an Farbstoffe gekoppelt sind, verwendet werden, um spezifische Proteine in den Zellen nachzuweisen. Diese Proteine dienen als „Marker“, die dem Pathologen helfen, die Krebsart zu bestätigen und den Ursprungsort zu bestimmen.
Das Adenokarzinom der Lunge zeigt typischerweise folgende Ergebnisse:
-
TTF-1: Positiv.
-
S. 40: Negativ.
-
CK5: Negativ.
-
Chromogranin: Negativ.
-
Synaptophysin: Negativ.
Dieses Färbemuster unterstützt die Diagnose und hilft, andere Arten von Lungenkrebs wie Plattenepithelkarzinome oder neuroendokrine Tumoren auszuschließen.
Histologische Typen des Adenokarzinoms
Das Adenokarzinom der Lunge wird anhand des Wachstumsmusters der Krebszellen in histologische Typen unterteilt. Ein Tumor kann ein oder mehrere Wachstumsmuster aufweisen.
Lepidischer Typ
Krebszellen wachsen entlang der Innenfläche der Alveolen. Ist der Tumor vollständig lepidisch und kleiner als 3 cm, wird er als AIS klassifiziert.
Azinärer Typ
Tumorzellen bilden runde, drüsenartige Strukturen.
Fester Typ
Tumorzellen wachsen in dichten Verbänden mit wenig Zwischenraum. Dieser Typ ist aggressiver.
Papillärer Typ
Tumorzellen bilden fingerartige Ausstülpungen, sogenannte Papillen.
Mikropapillärer Typ
Die Tumorzellen bilden winzige Ansammlungen, die Büscheln ähneln. Dies ist ein äußerst aggressives Wachstumsmuster.
Tumorgrad
Bei Lungenadenokarzinomen beschreibt der Tumorgrad, wie aggressiv der Krebs unter dem Mikroskop erscheint. Der Grad basiert auf zwei mikroskopischen Merkmalen:
-
Das vorherrschende histologische Muster.
-
Das schlimmste (aggressivste) Muster, das irgendwo im Tumor zu sehen ist.
Tumoren mit überwiegend lepidischem Wachstum und minimalen soliden oder mikropapillären Anteilen sind gut differenziert, d. h. sie wachsen langsamer und haben eine bessere Prognose. Tumoren mit azinärem oder papillären Wachstum und geringen Anteilen aggressiver Muster sind mäßig differenziert. Tumoren mit einem hohen Anteil solider oder mikropapillärer Anteile sind schlecht differenziert, d. h. sie verhalten sich aggressiver, wachsen schneller und neigen eher zur Metastasierung.
Der Tumorgrad ist einer der wichtigsten Prognosefaktoren, insbesondere im Frühstadium der Erkrankung.
Ausbreitung durch Lufträume (STAS)
STAS bedeutet, dass Krebszellen außerhalb des Haupttumors in den Lungenbläschen gefunden werden. Diese Zellen sind vom primären Tumor getrennt und können sich durch die kleinen Atemwege der Lunge bewegen.
Das Vorhandensein von STAS ist mit einem höheren Rezidivrisiko verbunden, insbesondere nach begrenzten chirurgischen Eingriffen wie der Keilresektion. Daher wird STAS im Pathologiebericht vermerkt und dient als Grundlage für die Therapieentscheidung.
Mehrere Tumore
Es ist möglich, mehrere Tumoren in der Lunge zu finden. In solchen Fällen wird jeder Tumor einzeln untersucht. Manchmal handelt es sich bei mehreren Tumoren um Metastasen eines ursprünglichen Tumors, insbesondere wenn sie unter dem Mikroskop identisch aussehen. Treten kleinere sekundäre Wucherungen in derselben Lunge wie der Primärtumor auf, werden sie oft als Knoten bezeichnet. Dabei handelt es sich um kleine, runde Läsionen, die eine Metastasierung innerhalb der Lunge darstellen können.
In anderen Fällen können die Tumoren unabhängig voneinander entstanden sein, insbesondere wenn sie unterschiedliche histologische Muster oder Merkmale aufweisen. Beispielsweise kann ein Tumor ein Adenokarzinom und ein anderer ein Plattenepithelkarzinom sein. Entstehen Tumoren unabhängig voneinander, gelten sie als separate primäre Karzinome und nicht als Metastasen. Die Unterscheidung zwischen diesen beiden Möglichkeiten ist wichtig, da sie Einfluss auf das Stadium, die Behandlung und die Prognose hat.
Pleurainvasion
Das Brustfell ist eine dünne Membran mit zwei Schichten:
-
Das viszerale Brustfell bedeckt die Oberfläche der Lunge.
-
Das parietale Blatt der Pleura kleidet die Innenseite der Brusthöhle aus.
Pleurainvasion bedeutet, dass Krebszellen in eine oder beide dieser Schichten eingewachsen sind. Tumoren, die nur die viszerale Pleura befallen, gelten als lokal fortgeschrittener als Tumoren, die auf das Lungengewebe selbst beschränkt sind. Tumoren, die die parietale Pleura – die äußere, an der Brustwand anliegende Schicht – befallen, gelten als noch fortgeschrittener, da der Krebs über die Lunge hinausgewachsen ist und das Brustfell erreicht hat. Pleurainvasion erhöht das T-Stadium und ist mit einem höheren Risiko für Ausbreitung und Rezidiv verbunden.
Lymphovaskuläre Invasion
Eine lymphovaskuläre Invasion (LVI) liegt vor, wenn Krebszellen in Blut- oder Lymphgefäße im oder in der Nähe des Tumors eindringen. Diese Gefäße dienen als Ausbreitungswege für den Krebs in andere Körperregionen, darunter Lymphknoten, Knochen, Leber oder Gehirn. Bei Vorliegen einer lymphovaskulären Invasion ist das Metastasierungsrisiko erhöht, und eine zusätzliche Behandlung kann empfohlen werden.
Die Margen
Als Resektionsränder bezeichnet man die Ränder des während einer Operation entfernten Gewebes. Der Pathologe untersucht alle Resektionsränder, um festzustellen, ob der Tumor vollständig entfernt wurde. Ein negativer Resektionsrand bedeutet, dass am Schnittrand keine Krebszellen nachweisbar sind. Ein positiver Resektionsrand bedeutet, dass sich am Rand Krebszellen befinden, was Anlass zur Sorge gibt, dass Krebszellen zurückgeblieben sind. Der Resektionsrandstatus hilft den Ärzten bei der Entscheidung, ob eine weitere Operation oder eine Strahlentherapie erforderlich ist.

Lymphknoten
Lymphknoten Es handelt sich dabei um kleine Immunorgane, die die Lymphflüssigkeit filtern. Lungenadenokarzinome streuen häufig in die Lymphknoten der Lunge und des zentralen Brustkorbs. Während einer Operation können Lymphknoten aus bestimmten anatomischen Regionen (sogenannten Lymphknotenstationen) entfernt und untersucht werden.
Der Pathologiebericht gibt die Anzahl der untersuchten Lymphknoten, deren Lage und das Vorhandensein von Krebszellen an. Diese Informationen helfen bei der Bestimmung des Lymphknotenstadiums und spielen eine wichtige Rolle bei der Wahl der Behandlung.

Pathologisches Stadium (pTNM)
Das Lungenadenokarzinom wird nach dem TNM-System klassifiziert:
-
Das T-Stadium beschreibt die Größe des Tumors und ob er in benachbarte Strukturen eingewachsen ist.
-
Das N-Stadium beschreibt, ob Lymphknoten Krebszellen enthalten.
-
Das M-Stadium beschreibt, ob sich der Krebs auf entfernte Organe wie Gehirn, Knochen oder Leber ausgebreitet hat.
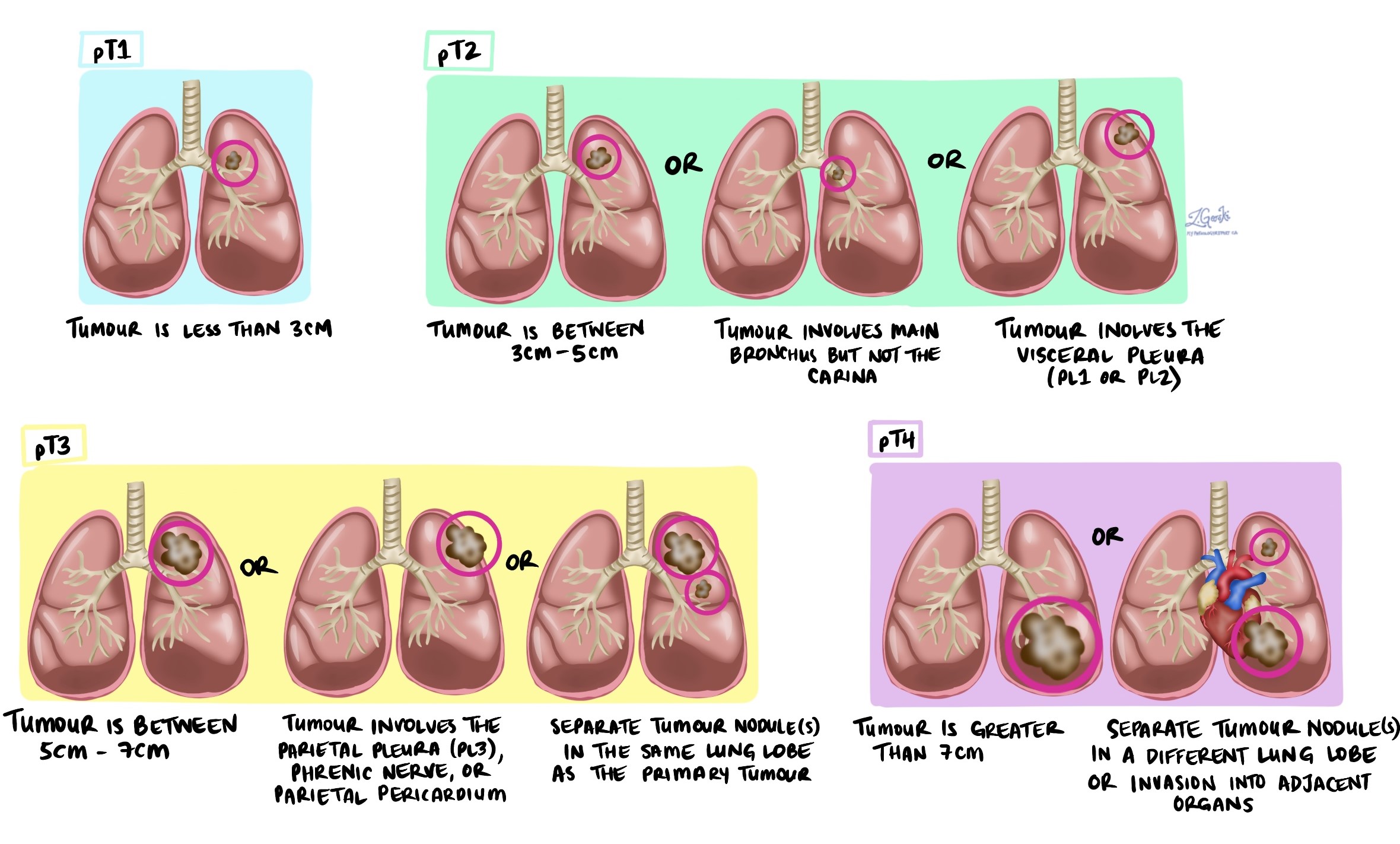
Tumorstadium (pT)
-
T1: Der Tumor ist 3 cm oder kleiner.
-
T2: Der Tumor ist größer als 3 cm, aber nicht größer als 5 cm, oder er hat die viszerale Pleura oder die zentralen Atemwege befallen.
-
T3: Der Tumor ist größer als 5 cm, aber nicht größer als 7 cm oder ist in benachbartes Gewebe eingewachsen.
-
T4: Der Tumor ist größer als 7 cm oder hat in nahegelegene Organe wie das Herz oder die Speiseröhre eingewachsen.
Knotenstadium (pN)
-
NX: Die Lymphknoten wurden nicht untersucht.
-
N0: Keine Krebszellen in den Lymphknoten.
-
N1: Krebszellen in Lymphknoten innerhalb der Lunge oder in der Nähe der Atemwege (Stationen 10–14).
-
N2: Krebszellen in Lymphknoten im zentralen Brustkorb in der Nähe der Atemwege (Stationen 7–9).
-
N3: Krebszellen in Lymphknoten auf der gegenüberliegenden Seite des Brustkorbs oder im unteren Halsbereich (Stationen 1–6).
Höhere Stadien bergen ein höheres Risiko der Ausbreitung und des Wiederauftretens und erfordern oft eine intensivere Behandlung.
Biomarker für Adenokarzinom der Lunge
Biomarker sind messbare Veränderungen in Krebszellen, die häufig spezifische Gene oder Proteine betreffen. Diese Veränderungen helfen Ärzten, das Verhalten des Tumors zu verstehen und die erfolgversprechendsten Behandlungen auszuwählen. Beim Lungenadenokarzinom sind Biomarker besonders wichtig, da viele Tumoren genetische Veränderungen aufweisen, die mit Therapien gezielt behandelt werden können, indem die abnormalen Signale blockiert werden, die das Krebswachstum fördern. Biomarker-Tests gehören heute zur Standarddiagnostik und sind maßgeblich für viele Behandlungsentscheidungen.
Welche Arten von Biomarkern werden bei Lungenadenokarzinomen getestet?
Die meisten Biomarker-Tests bei Lungenadenokarzinom konzentrieren sich auf genetische Mutationen und Genumlagerungen in der Tumor-DNA. Diese Veränderungen werden mithilfe spezieller Labortechniken wie PCR (einem Test zur Vervielfältigung kleiner DNA-Abschnitte), Next-Generation-Sequenzierung (NGS; einem Test zur gleichzeitigen Untersuchung vieler Gene) und FISH (einem Test, der fluoreszierende Sonden zum Nachweis von Genumlagerungen verwendet) nachgewiesen. Diese Tests werden an Biopsiegewebe oder dem während der Operation entfernten Tumor durchgeführt und spielen eine entscheidende Rolle bei der Bestimmung der wirksamsten Behandlungsoptionen.
EGFR
EGFR ist ein Gen, das für einen Rezeptor kodiert, der das Zellwachstum reguliert. Bei bestimmten Mutationen im EGFR-Gen wird der Rezeptor überaktiv und fördert so das Tumorwachstum. EGFR-Mutationen treten häufig bei Nichtrauchern, Frauen und Menschen ostasiatischer Abstammung auf. Diese Mutationen sind von Bedeutung, da Tumoren mit EGFR-Veränderungen oft sehr gut auf EGFR-gerichtete Therapien ansprechen. Diese Therapien blockieren das abnorme Wachstumssignal und können den Tumor verkleinern oder sein Fortschreiten verlangsamen.
Pathologen testen auf EGFR-Mutationen, indem sie die DNA des Tumors mittels PCR oder Next-Generation-Sequenzierung untersuchen, um spezifische genetische Veränderungen zu erkennen.
Im Pathologiebericht wird der Tumor als EGFR-positiv beschrieben, wenn eine Mutation nachgewiesen wird, und als EGFR-negativ, wenn keine Mutation gefunden wird.
ALK
Das ALK-Gen kann mit einem anderen Gen fusionieren und so ein abnormales Fusionsprotein bilden, das das Tumorwachstum fördert. Diese ALK-Fusionen treten häufiger bei jüngeren Patienten und Nichtrauchern auf. ALK-Rearrangements sind von Bedeutung, da Tumoren mit dieser Veränderung oft sehr gut auf ALK-gerichtete Therapien ansprechen, welche das abnormale Fusionsprotein blockieren.
Die ALK-Testung erfolgt mittels Immunhistochemie, die das ALK-Protein in Tumorzellen hervorhebt, FISH, die ALK-Genumlagerungen nachweist, oder Next-Generation-Sequenzierung, die das ALK-Gen direkt analysiert.
Tumoren werden als ALK-positiv bezeichnet, wenn eine Rearrangierung vorliegt, und als ALK-negativ, wenn keine Rearrangierung gefunden wird.
ROS1
ROS1 ist ein Gen, das sich umlagern und ein Fusionsprotein bilden kann, welches das Tumorwachstum fördert. Obwohl ROS1-Fusionen seltener vorkommen als EGFR- oder ALK-Mutationen, sind sie dennoch wichtig, da sie sehr gut auf ROS1-gerichtete Therapien ansprechen, welche das abnorme Protein blockieren und so zur Krebskontrolle beitragen.
Der Nachweis von ROS1 kann mittels Immunhistochemie, FISH oder Next-Generation-Sequenzierung erfolgen.
Ihr Tumor wird als ROS1-positiv bezeichnet, wenn eine Fusion gefunden wird, und als ROS1-negativ, wenn keine Fusion gefunden wird.
BRUDER
BRAF ist ein Gen, das an der Regulierung des Zellwachstums beteiligt ist. Bestimmte Mutationen, wie beispielsweise die BRAF-V600E-Mutation, können zu einem beschleunigten Wachstum von Tumorzellen führen. Diese Mutationen sind von Bedeutung, da Tumore mit BRAF-Veränderungen auf BRAF-gerichtete Therapien ansprechen können, welche den abnormalen Signalweg blockieren.
Die Tests werden durchgeführt, indem die Tumor-DNA mittels PCR oder Next-Generation-Sequenzierung analysiert wird, um spezifische BRAF-Mutationen zu identifizieren.
Ihr Tumor wird als BRAF-positiv bezeichnet, wenn eine Mutation vorliegt, und als BRAF-negativ, wenn keine Mutation nachgewiesen wird.
MET
MET ist ein Gen, das das normale Zellwachstum reguliert. Eine spezifische Genmutation, das MET-Exon-14-Skipping, führt dazu, dass das MET-Protein länger als üblich aktiv bleibt und Tumorzellen ungehindert wachsen können. Dieser Biomarker ist wichtig, da Tumore mit MET-Exon-14-Skipping häufig auf MET-gerichtete Therapien ansprechen.
Die MET-Testung wird üblicherweise mittels Next-Generation-Sequenzierung durchgeführt, um das Überspringen von MET-Exon 14 oder andere MET-Mutationen nachzuweisen.
Ihr Tumor wird als MET-positiv eingestuft, wenn eine MET-Mutation nachgewiesen wird, und als MET-negativ, wenn keine Mutation gefunden wird.
RET
Das RET-Gen kann mit einem anderen Gen fusionieren und so ein abnormales Protein bilden, das das Tumorwachstum fördert. RET-Fusionen sind von Bedeutung, da Tumore mit dieser Veränderung oft außergewöhnlich gut auf RET-gerichtete Therapien ansprechen.
RET-Fusionen werden mittels Next-Generation-Sequenzierung oder FISH identifiziert, die beide die abnorme Umlagerung nachweisen können.
Ihr Tumor wird als RET-positiv bezeichnet, wenn eine Fusion vorliegt, und als RET-negativ, wenn keine Fusion vorliegt.
NTRK (NTRK1, NTRK2, NTRK3)
NTRK-Gene können mit anderen Genen fusionieren und so abnorme TRK-Fusionsproteine bilden, die das Tumorwachstum stark fördern. Obwohl selten, sind diese Fusionen von Bedeutung, da Tumoren mit NTRK-Veränderungen häufig ein dramatisches und lang anhaltendes Ansprechen auf TRK-gerichtete Therapien zeigen.
Die NTRK-Testung kann eine Immunhistochemie zum Screening auf abnorme TRK-Protein-Expression umfassen, gefolgt von FISH oder Next-Generation-Sequenzierung zur Bestätigung des Vorhandenseins einer Genfusion.
Ihr Tumor wird als NTRK-positiv bezeichnet, wenn eine Fusion gefunden wird, und als NTRK-negativ, wenn keine Fusion festgestellt wird.
KRATZEN
KRAS ist ein Gen, das an der Regulation von Zellwachstum und -teilung beteiligt ist. KRAS-Mutationen zählen zu den häufigsten Biomarkern beim Lungenadenokarzinom, insbesondere bei Menschen mit einer Raucheranamnese. Diese Mutationen sind von Bedeutung, da sie die Vorhersage des Tumorverhaltens ermöglichen und die spezifische KRAS-Mutation KRAS G12C mit neuen, auf KRAS abzielenden Medikamenten behandelt werden kann.
KRAS-Mutationen werden mittels PCR oder Next-Generation-Sequenzierung durch Analyse der Tumor-DNA nachgewiesen.
Ihr Tumor wird als KRAS-positiv bezeichnet, wenn eine Mutation nachgewiesen wird, und als KRAS-negativ, wenn keine Mutation gefunden wird.
ERBB2 (HER2)
ERBB2, auch bekannt als HER2, ist ein Gen, das Mutationen aufweisen kann, die zu abnormaler Signalübertragung und Tumorwachstum führen. HER2-Veränderungen sind von Bedeutung, da zielgerichtete Therapien – und laufende klinische Studien – Tumore mit HER2-Mutationen behandeln.
Die HER2-Testung erfolgt mittels Next-Generation-Sequenzierung, um ERBB2-Mutationen in der DNA des Tumors nachzuweisen.
Ihr Tumor wird als ERBB2-positiv bezeichnet, wenn eine Mutation nachgewiesen wird, und als ERBB2-negativ, wenn keine Mutation nachgewiesen wird.
NRAS
NRAS ist ein Gen, das dem KRAS-Gen ähnelt und an Zellwachstumsprozessen beteiligt ist. NRAS-Mutationen treten häufiger bei Rauchern auf. Obwohl es noch keine spezifischen NRAS-gerichteten Therapien gibt, hilft der Nachweis einer NRAS-Mutation Ärzten, das Tumorverhalten zu verstehen und die Teilnahme an klinischen Studien zu prüfen.
Die NRAS-Testung erfolgt mittels Next-Generation-Sequenzierung, um nach Mutationen in der DNA des Tumors zu suchen.
Ihr Tumor wird als NRAS-positiv bezeichnet, wenn eine Mutation nachgewiesen wird, und als NRAS-negativ, wenn keine Mutation gefunden wird.
MAP2K1 (MEK1)
MAP2K1, auch MEK1 genannt, ist ein Gen, das an einem Signalweg beteiligt ist, der das Zellwachstum reguliert. Mutationen in MAP2K1 sind von Bedeutung, da gezielte Therapien, die auf diesen Signalweg abzielen, erforscht werden und möglicherweise zukünftige Behandlungsoptionen darstellen.
Die MAP2K1-Testung erfolgt mittels Next-Generation-Sequenzierung, um Mutationen in der Tumor-DNA nachzuweisen.
Ihr Tumor wird als MAP2K1-positiv bezeichnet, wenn eine Mutation nachgewiesen wird, und als MAP2K1-negativ, wenn keine Mutation gefunden wird.
NRG1
NRG1 ist ein Gen, das Umlagerungen oder Fusionen eingehen kann, die das Tumorwachstum fördern. Obwohl selten, sind NRG1-Umlagerungen von Bedeutung, da sie möglicherweise auf neue und vielversprechende, derzeit in der Erforschung befindliche NRG1-gerichtete Therapien ansprechen.
Bei der NRG1-Testung wird die DNA des Tumors mittels Next-Generation-Sequenzierung auf Anzeichen einer Genumlagerung untersucht.
Ihr Tumor wird als NRG1-positiv bezeichnet, wenn eine Umlagerung festgestellt wird, und als NRG1-negativ, wenn keine Umlagerung gefunden wird.
PD-L1
PD-L1 ist ein Protein auf der Oberfläche einiger Krebszellen. Es interagiert mit Immunzellen und ermöglicht dem Tumor so, dem Immunsystem zu entgehen und nicht zerstört zu werden. PD-L1 ist wichtig, da Tumoren mit hoher PD-L1-Expression eher auf eine Immuntherapie ansprechen – eine Behandlungsform, die das Immunsystem dabei unterstützt, Krebszellen zu erkennen und anzugreifen. Immuntherapeutische Medikamente, sogenannte PD-1- oder PD-L1-Inhibitoren, gehören heute zur Standardtherapie für viele Patienten mit Lungenadenokarzinom, insbesondere wenn der Tumor hohe PD-L1-Werte aufweist.
Pathologen untersuchen PD-L1 mittels Immunhistochemie, einer Labormethode, bei der Antikörper, die mit Farbstoffen gekoppelt sind, an das PD-L1-Protein binden und es unter dem Mikroskop sichtbar machen. Der Test misst, wie viele Tumorzellen PD-L1 auf ihrer Oberfläche aufweisen und wie stark sie es exprimieren. Dieser Test wird üblicherweise an einer Biopsieprobe vor Behandlungsbeginn durchgeführt.
Die PD-L1-Ergebnisse werden als Prozentsatz angegeben und stellen den Anteil der Tumorzellen dar, die eine PD-L1-Färbung aufweisen. Dies wird als Tumorproportion-Score (TPS) bezeichnet.
-
Ein TPS-Wert von <1 % wird als PD-L1-negativ oder sehr niedrig eingestuft.
-
Ein TPS-Wert von 1–49 % wird als niedrige bis mittlere Expression angesehen.
-
Ein TPS-Wert von 50 % oder höher gilt als hohe Expression.
Je nach verwendeter Testmethode können in einigen Berichten auch Werte für Immunzellen angegeben oder der kombinierte positive Wert (CPS) verwendet werden.
Nach der Diagnose
Nachdem Ihre Diagnose bestätigt wurde, wird Ihr Arzt den Pathologiebericht, die Bildgebungsbefunde und Ihren allgemeinen Gesundheitszustand auswerten, um einen individuellen Behandlungsplan zu erstellen. Die Behandlung kann eine Operation, Chemotherapie, Immuntherapie, zielgerichtete Therapie, Strahlentherapie oder eine Kombination dieser Verfahren umfassen.
Es ist wichtig, dass Ihr Tumor molekulargenetisch untersucht wird. Viele Lungenadenokarzinome weisen spezifische genetische Veränderungen auf, wie beispielsweise Mutationen in den Genen EGFR, ALK, ROS1, KRAS oder RET, die mit hochwirksamen Therapien gezielt behandelt werden können. Molekulargenetische Untersuchungen sind heute ein Standard und unverzichtbarer Bestandteil der Lungenkrebsbehandlung, selbst im Frühstadium.
Ihr Behandlungsteam wird möglicherweise auch weitere bildgebende Verfahren zur Feststellung einer Ausbreitung, Lungenfunktionstests zur Beurteilung Ihrer Lungenkapazität und Strategien zur Linderung von Symptomen wie Husten oder Atemnot mit Ihnen besprechen. Nachsorgeuntersuchungen nach der Behandlung sind wichtig, um ein Wiederauftreten der Erkrankung oder die Entwicklung neuer Lungenknoten zu überwachen.
Fragen an Ihren Arzt
-
In welchem Stadium befindet sich mein Krebs und was bedeutet das für meinen Behandlungsplan?
-
Wurde in meinem Tumor eine Pleurainvasion, eine lymphovaskuläre Invasion oder eine STAS festgestellt?
-
Waren die Operationsränder klar?
-
Hat sich der Krebs auf Lymphknoten ausgebreitet?
-
Benötige ich molekulargenetische Tests auf EGFR, ALK, KRAS oder andere Biomarker?
-
Welche Behandlungen empfehlen Sie und welche Ziele verfolgen sie?
-
Sollte ich zur weiteren Behandlung einen medizinischen Onkologen, Strahlentherapeuten oder Chirurgen aufsuchen?
-
Welchen Nachsorgeplan empfehlen Sie nach der Behandlung?